栾素娴医生的科普号
- 精选 三倍体遗传咨询
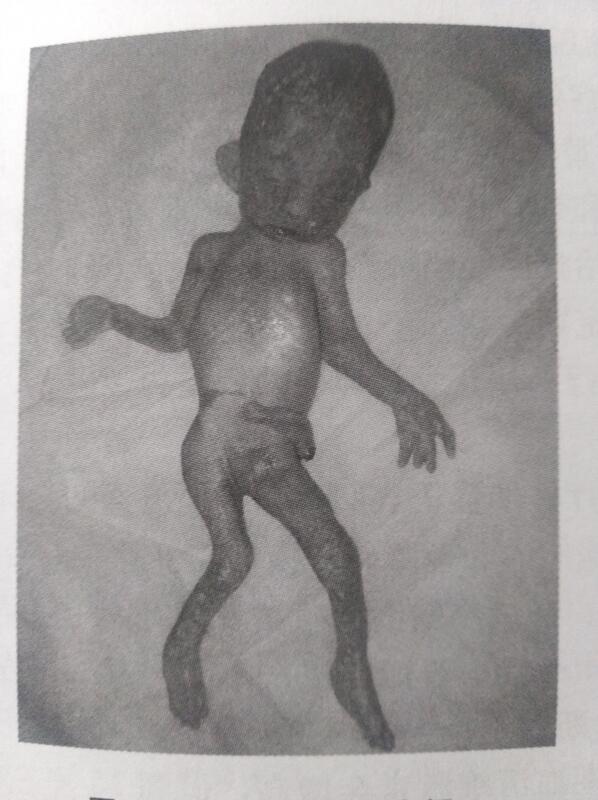
三倍体,产前诊断中比较常见的一种多倍体,核型有三中69XⅩⅩ,69ⅩXY,69XYY,机制主要是双雄受精,和双雌受精。 特征性表现:大胎盘伴葡萄样变,发育障碍,第三 四并指。 三倍体的表型与基因组印迹相关。通常,父源性基因的表达影响胎盘的发育,母源性基因的表达对胚胎的发育更为重要。父源性三倍体常表现为中孕期以后常见的局部性葡萄样发育的囊状大胎盘,母源性三倍体则以早期自然流产或严重胎儿发育障碍,头大身小,胎盘细小不发育但无葡萄样变等为特点。 风险评估与预防: 1:双雌受精性三倍体的再发风险不升高,双雄受精性三倍体的再发生风险为1%一3% 2:再次妊娠要警惕恶性葡萄胎的出现 3:妊娠过程中出现胎儿生长受限胎盘增厚和小水泡样改变现象时,要注意与一般胎儿生长受限 胎盘早剥和父源性单亲二倍体引起的完全性葡萄胎进行鉴别 4:在高度怀疑三倍体综合征时,建议羊水细胞染色体核型分析确诊,并尽早终止妊娠。
 栾素娴 副主任医师 潍坊市人民医院 生殖医学中心5人已购买
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心5人已购买 - 精选 HCG检测有哪些作用?
一、HCG的产生与正常变化 HCG 绒毛膜促性腺激素是受精卵滋养层形成(受精后第6日)时开始分泌的,开始分泌微量,受精后10日能在母血中检出。受精卵植入1周内,血清β-hCG水平从5IU/L上升至50IU/L。植入后14日约100IU/L。正常妊娠前6周,HCG水平约36~48小时增长一倍。妊娠6周后,当HCG水平达到6000~10000IU/L时,HCG上升速度开始减慢。注意上升速度减慢 不是降低。 HCG于妊娠8~10周达到高峰,约为100000~200000IU/L,持续10日后(约1~2周)迅速下降,约在妊娠20周下降到最低值,持续至分娩;产后明显降低,分娩后若无胎盘残留,约在产后2周内降至正常水平。中、晚妊娠时,血HCG浓度约为高峰时的10%。 二、哪些情况HCG会出现异常降低 自然流产、异位妊娠时,HCG水平通常低下。 妊娠早期,HCG增加迅速,倍增时间约为1.4~2.2日。一般认为,正常宫内妊娠,血清β-hCG水平每天最低或至少增长24%,2天至少增长53%,故妊娠早期可动态测定β-hCG水平,利用倍增特点判断预后。 当初始HCG水平低于2000IU/L时,若为正常宫内妊娠,48小时的HCG水平多数倍增;若48小时HCG水平增幅低于50%,HCG水平仍未达到2000IU/L,提示胚胎死亡。(此处备注 要参考不同医院化验室的参考值。) 通常,完全流产时,HCG水平明显下降(48小时HCG水平下降超过50%)。 异位妊娠时,HCG值通常比正常妊娠时低。动态测定HCG,若无阴道流血,48小时HCG上升少于50%,或血HCG下降缓慢,半衰期大于1.4天,异位妊娠风险增大;如β-HCG>2000IU/L,阴道B超未在宫腔内探到孕囊,多可诊断为异位妊娠。 三、哪些情况HCG会出现异常增高 多胎妊娠、Rh血型不合溶血的单胎妊娠、葡萄胎或绒毛膜癌,母体血清HCG水平异常增高。 妊娠中期,唐氏综合症胎儿母体血清Free-HCG水平也异常增高,因此,HCG可作为产前筛查的血清生化标志物。 葡萄胎时,滋养细胞高度增生,产生大量HCG,血清HCG滴度通常高于相应孕周的正常妊娠值;而且在停经12周以后,随着子宫增大继续持续上升,HCG在10000IU/L以上,常超过100000IU/L,且持续不降,利用这种差别可辅助诊断。 在正常情况下,葡萄胎排空后,HCG稳定下降,首次降至正常的平均时间约为9周,最长不超过14周。葡萄胎排空9周以上,或流产、足月产、异位妊娠后4周以上血HCG值持续高水平,或曾一度下降后又上升,排除妊娠物残留或再次妊娠,结合临床表现可诊断为滋养细胞肿瘤。 四、HCG检测的其他作用 若HCG水平正常翻倍上升,当HCG水平达到1000~1800IU/L时,阴道超声检查能显示大多数宫内妊娠,宫腔内可见2~4mm液性暗区(孕囊)。 β-hCG1800~2300IU/L时,经阴道超声可100%显示宫内孕囊。根据β-hCG的变化可预测妊娠失败。β-hCG比(β-hCG48h:0h)<0.87(或β-hCG下降>13%),预测妊娠失败的敏感性92.7%,特异性96.7%。β-hCG比>2,预测未确定位置妊娠最后为宫内活胎妊娠的敏感性为77.2%、特异性为95.8%、PPV86.6%、NPV90.9%。 在人工受精后第16~18天,若HCG水平可达到300IU/mL,获得活胎机会有88%;若HCG水平<300IU/mL,获得活胎机会降低为22%。 非妊娠期出现HCG,提示存在直接或异位分泌此种激素的肿瘤,如葡萄胎、侵蚀性葡萄胎、绒毛膜癌、卵巢未成熟畸胎瘤、卵巢无性细胞瘤、卵巢腺癌、下丘脑绒毛膜瘤、肝胚胎瘤、肝癌、肠癌、胰腺癌、胃癌、肺癌、乳腺癌、肾癌等等。
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心2478人已读 - 精选 关于OHSS
OHSS病理生理:在辅助生殖技术中促排卵是其中重要的步骤,其中一定程度的卵巢刺激时必要的,然而过度的反应性可能导致有潜在生命危险的过度卵巢刺激,卵巢过激的平均发生率在3~6%,在所有周期中重度的发生率是0.1~3%,卵巢过激在所有的辅助生殖技术中,在克罗米芬的周期中或是自发妊娠中也有可能出现。卵巢过激的高危因素如下:年轻小于35岁,BMI低,大剂量的外源性促性腺激素,E2水平较高或是增长过快,以前的过激病史,治疗不育症的内科医师应该充分了解OHSS的病理生理,尽量避免这种医源性疾病。血管通透生增高和卵巢增大是所有的共性,液体从血管渗出到第三腔隙导致低血容量,轻度的卵巢增大缺乏临床的参考意义,重度者特征是卵巢增大、胸腔积液、腹水、积液、血液浓缩、血栓形成如表1 雌激素:雌激素在OHSS的病理生理中占有重要的位置,作为当时一种高水平的性激素与OHSS的症状有很大的关联,这种关联使人们相信高浓度的雌激素水平导致此种过激的症状,然而,有证据表明,雌激素对OHSS不是必要的条件,有一17、20单甾裂解酶缺乏的妇女,尽管她雌激素水平很低但是在辅助生殖技术中也发生了卵巢过度刺激。单纯高水平的雌激素并不导致过激,只有在HCG也迅速升高的情况下.现在高雌激素水平与过激的相关性, 仅仅表示高雌激素代表颗粒细胞功能活跃,尽管如此,高浓度的雌激素仍然被认为是卵巢过激的最好的预测指标。HCG早辅助生殖技术中常用来刺激lh受体,激发lh峰水平,促进卵泡最后阶段的发育和成熟,HCG的生物活性是lh的6~7 倍,由于其较长的半衰期,对受体的亲和力更长久。高浓度的HCG水平是OHSS启动的基础,但并非必须。有人评估了27名HCG水平超过150000IU/L的妊娠妇女,均没有自发的发展为OHSS,但是在同期杂志上,也报道了一例36岁妇女自然自然妊娠在10周妊娠时发生OHSS的个案,以前已经出现过4例这样的相关报道。Inflammatory mediators炎性介质:在OHSS的病理生理中有许多免疫系统的产物,在卵泡最后成熟阶段、排卵、黄体功能和胚胎植入的过程中伴发的炎症反应中有许多的细胞因子,在许多OHSS病人中发现白介素的浓度较高,其中白介素6的表达较高,后者与血管的渗透性、血液浓缩、血浆高雌激素水平有关、同时抑制肝脏产生白蛋白。Renin-angiotensin system血浆肾素活性与OHSS严重程度的直接相关性在20年前就已经很清楚了,卵巢能够合成肾素的前体-肾素原和肾素,此外, 在OHSS的病人中卵泡囊肿和腹水中血管紧张素的浓度远远高于血浆中的浓度, 已经报道了在一例重度OHSS患者中发现血浆中的血管紧张素转化酶浓度较高,然而,肾素-血管紧张系统活性可能影响OHSS但不能导致OHSS,低血容量与由肾素血管紧张素引发的高醛固酮血症有关的 。Vascular endothelial growth factor (VEGF):通过对啮齿类动物的研究,证实OHSS患者在性腺激素刺激阶段和后续的HCG注射阶段中,血管渗透性、VEGF和VEGF受体存在较高的水平。然而,这些参数的进一步变化受HCG水平的影响,随之而来的刺激,VEGFR只有在黄体血管中存在,但是在HCG刺激后,这些受体在黄体的所有组织中都能找到,另外,VEGF and VEGFR在HCG注射后48小时浓度达高峰,VEGF通过改变上皮连接蛋白之间的结构,增加血管渗透性, 包括钙黏连蛋白、和肌调节蛋白5。当以脐静脉血管作为OHSS的模型时,HCG和VEGF改变 肌动蛋白,后者是增加血管渗透性,当HCG和VEGF增加时,钙黏蛋白浓度升高,但是并不伴随雌激素的增加, 最近一项通透血管模型(黄体颗粒细胞和胎儿脐静脉上皮细胞)研究表明HCG导致VEGF浓度升高和血管渗透性增加,这和内皮细胞上claudin 5表达减少相关,. Prevention strategies:预防措施:预防OHSS最重要的方面是临床对高危因素的判断,在面对高危因素的局面下,有许多步骤可供参考 (Table 2).Coasting 滑行;是指针对高雌激素水平的患者延缓应用HCG,直到有个较安全的雌激素水平时。在这个阶段应该停止或是减少促性腺激素,在一项回顾性的研究中高风险的妇女停止Gn最少3天血浆中雌激素的浓度会降低63% (from 18,043 to 6,656 pmol/L),而继续接受Gn的高危妇女只减少了 29% (from 14,205 to10,132 pmol/L)。关于滑行,停止Gn,最多3天,会降低OHSS的风险,但是不会影响妊娠率。然而,停止4天或超过以上天数,会导致较低的胚胎种植率,原因可能是影响子宫内膜的容受性。是否应用滑行通常由应用Gn时血浆雌激素水平决定的,不过,什么时候应该应用Gn,目前还没有一致意见,许多文章认为雌激素的最低切割值在 2,500 and 4,000 pg/ml之间。滑行预防OHSS的理论尚不明确,卵巢所有卵泡尤其是直径小于14mm的卵泡的凋亡增加被认为可能是滑行理论的机制,原因是上述卵泡是血浆中高浓度雌激素和血管活性物质的首要因素, 滑行之后随之而来的是血清雌激素和卵泡分泌表达的VEGF的减少,尽管滑行在预防OHSS中是比较普通的步骤,但是确实被认为最有意义的,原因是滑行后血清雌激素浓度显著降低,目前尚缺乏关于滑行与不滑行的RCT研究. 证实滑行是OHSS有效地预防措施的证据尚不充分,即使滑行OHSS的发生率仍高达9、4%。Albumin administration 白蛋白的治疗:白蛋白是一种低分子量的血浆复合物, 对血浆胶体渗透压由主要的影响。人白蛋白在OHSS高危妇女中是在HCG应用日开始应用以预防OHSS的发生,然而, 它的有效性仍是很有争议的,2002年的一篇综述总结了5个RCT研究,在193名妇女应用白蛋白,185名妇女为对照组,白蛋白组OHSS的发生率是0.28 (95%IC 0.11–0.73).,根据该研究,18名高危妇女有必要进一步预防可能发生的OHSS。然而,后继的临床研究并没有显示应用白蛋白的益处。在众多的研究中,一项RCT包括998名高危妇女, 一组是取卵后即刻给予40g白蛋白,对照组不采取治疗措施,连续7天的治疗后,对比两组在血液浓缩、肝肾功能障碍、中或重度OHSS的发生几率都没有明显的区别,(the incidences of moderate-severe and severeonlyOHSS were identical between the groups 两组中重度和重度OHSS的发生率完全相同). 作者结论取卵时给予白蛋白对预防OHSS没有用处。Renin-angiotensin system blockade RAS系统的阻断:已经报道的两组病例说明了双重阻断的应用,即血管紧张素受体阻滞剂和血管紧张素转化酶抑制剂的联合应用,在这两项研究中,14名高危妇女 (雌二醇>8,000 pg/ml)参与研究,2名发展为中重度OHSS (14.4%).这两项研究中,胚胎被重新冻存,在下个周期进行移植,然而, 肾素-血管紧张素的激活可能是OHSS的结果而不是原因,当考虑到这个阶段是就应该小心,因为这不但对即将妊娠的胎儿有害,而且可能加重OHSS,导致肾衰竭。Dopamine agonist administration多巴胺激动剂的应用在动物模型中发现多巴胺激动剂卡麦角林可以抑制局部卵巢VEGF受体磷酸化水平并且它的后继作用可以对抗VEGF2血管渗透性,不影响黄体的血管生成,卡麦角林成为临床研究的目标,一项随机对照临床研究——取卵后卡麦角林0.5mg每天连用3周为研究组,对照组不采取措施.结果表明,两组的妊娠率、种植成功率、流产率几乎相同,早期OHSS率 (HCG应用后9天之内出现OHSS)研究组明显低于对照组, (0.0% vs. 14.5%). 晚发OHSS(10天以后)两组没有区别,治疗组是 10.8% ,对照组 3.6% ,全部OHSS发生率分别是—卡麦角林组10.8% 对照组18.1%。Non-steroidal anti-inflammatory administration非甾体抗炎药物的应用:最近的一项RCT研究表明,小剂量阿司匹林(卵巢刺激的第一天开始给予100mg每天)在高危妇女中应有有预防OHSS的作用,这项研究评估了 2,425个应用GnRHa的周期,有1,192 名高危OHSS风险的妇女,其中780名随机接受了阿司匹林,OHSS的发生率是0.25% 对照组 8.4% (剩余未接受阿司匹林治疗的) ,两组妊娠率相似。Meloxican 是另一种非甾体抗炎药物,该药物在动物模型中研究表明可通过减少卵巢体积和VEGF表达降低OHSS发生。GnRH antagonist protocol:GnRH拮抗剂方案GnRH拮抗剂可以直接抑制促性腺激素的分泌,它们通常用在外源性激素开始刺激之后,并可缩短治疗的持续时间, A recent meta-analysis [39] reported a discreet worsening in pregnancy rates when GnRH antagonistregimens were compared to the standard long protocol(OR=0.83; 95% CI=0.72–0.95), 最近一项研究表明,GnRH拮抗剂的样本与标准长方案相比较,妊娠率有点下降,据报道与其他预防OHSS的措施相同,重度OHSS明显减少,(OR=0.60, 95% CI 0.40–0.88) as well as fewer interventions to prevent OHSS (OR=0.43, 95% CI 0.20–0.92). 另外,因为这种药物在刺激卵巢时不被用来阻断垂体分泌功能,所以当应用GnRH拮抗剂方案可以用GnRH激活剂诱导卵泡成熟, This issue will be discussed later.本刊以后将讨论这些问题。Reducing HCG dosage:减少HCG的用量:就促排卵而言,以前的HCG的剂量时1万单位,现在一种渐减少的剂量逐渐被推荐,范围是5,000 到 2,500 IU. 在250个周期的回顾性研究中,HCG的习惯和一种减少的剂量3,300单位相比较,两者都是用于血清雌二醇浓度在 4,000 and 5,500 pg/mL, 卵泡的成熟率、受精率、妊娠率在两组间没有明显区别。这表明降低HCG用量,不影响IVF的结局。最近,一项关于在21名高危妇女中应用HCG2,500单位的安全性与有效性的实验性研究的评估中发现,没有发现中重度的OHSS,并且有较高的妊娠率 (61.9%),据此作者认为减少HCG用量的做法不影响IVF的结局同时可以降低OHSS的发生率。Eliminate HCG:清除HCG既然没有HCG这种激素的应用就没有观察到中重度的OHSS,那么从理论上讲如果不用HCG,OHSS的并发症可以消失, 重组lh可能是HCG的一种安全的代用品, 但是应用重组的lh在经济上不可行。 虽然如此, 5,000单位的HCG相当于重组的lh剂量在15,000 and 30,000 IU 。在GnRh拮抗剂方案中GnRh激动剂可以用来代替HCG诱导卵泡成熟,以GnRh激动剂取代HCG在经济上是可行的,同时还有较高的妊娠率,而且会降低中重度OHSS的发生率,两项回顾性队列研究,评估了2,289个卵子捐献者的卵巢刺激周期,回顾性分析了2,077个周期,和 212个RCT周期—比较HCG和GnRH激动剂诱导卵泡最后成熟的作用。结果表明后者中重度OHSS明显降低,应用激动剂没有过激的报道,而HCG中有14例报道,(回顾性分析中13例,RCT中1例)。另一明显的区别是回顾性分析中激动剂的受精率轻微增加 (65% vs. 69%; HCG组 vs. GnRH 激动剂组),这种现象在RCT中也有(67.8% vs. 71.1%), 但是这种区别没有统计学意义。在应用GnRH激动剂而不是HCG的高危妇女中没有中重度OHSS的报道,在一项随机临床对照研究中,评估了66名PCOS的高危妇女或以前有高敏感反应者,这些妇女被随机分为标准长GnRH诱导方案中HCG和GnRH激动剂最后诱导卵泡成熟两组 ,只有HCG组的妇女出现各种形式的OHSS,(31%, 10 of 32).在以下妊娠结局的相关因素中-种植率 (36.0% vs. 31.0%, GnRH激动剂组vs. HCG组, respectively), 临床妊娠率 (56.7%vs. 51.7%, respectively), 或者是持续的妊娠率(53.3% vs. 48.3%, respectively).并没有发现明显的区别。另一项研究是一项对42名妇女进行的回顾性的观察,这些妇女均是PCOS患者,她们以前均有因为OHSS风险而被取消周期的经历, 这些妇女接受拮抗剂方案,GnRH激动剂诱导卵泡最后成熟:所有的人都完成了取卵,没有人发展为OHSS。 胚胎均被冷冻,后来进行的植入。In vitro maturation of oocytes (IVM)体外卵细胞成熟预防OHSS最安全的方式是不要刺激卵巢,在IVM 周期中,不成熟的卵母细胞都是从刚刚受到刺激或是完全未受刺激的卵巢, 卵母细胞在固定的培养基内培养24至48小时成熟后,然后通过体外受精或是IGSI方式受精,胚胎移植还是和往常一样;通常2个胚胎在受精后2天或是3天进行移植,在IVM周期卵巢不受到刺激可以有许多好处,包括以下几点:减少药品的费用,没有OHSS的风险,减少了病人反复进行临床和实验室评估的次数。在PCOS的妇女中进行IVM的临床实验证实在胚胎移植中有较高的妊娠率,(20–54%),和较好的胚胎移植率(5.5–34.5%).当应用于有排卵的妇女中,结果不理想,每移植成功率中妊娠率是15至 33.3%,植入成功率是 8.8至 22.6%。有文献报道,大约400名孩子是IVM中诞生的,他们出生后的后续研究表明是可以放心 的,妊娠率的升高最近有报道认为是由于较好的实验室条件和临床策略,在取卵前应用HCG可以导致较高的卵泡成熟率,良好的内膜准备可以导致较高的植入率,这可以在每个胚胎移植率中要取得较高的妊娠率,高达40%.尽管临床报道好的结果,但是IVM还没有成为受精治疗的主流。重要的原因是: 1-从没有受到刺激的卵巢中取得未成熟的卵母细胞并培养有一定的技术难度; 2 – 与传统的IVF治疗相比,活胎的几率较低,3- 有报道称人类未成熟的卵母细胞中减数分裂纺锤体异常和染色体异常率较高。 Conclusions结论:OHSS的发生在辅助生殖技术是最严重的并发症,为取卵而进行的卵巢刺激不光是昂贵的而且给所有人沉重的感情负担,降低OHSS风险是关键的环节,尤其是针对那些被认为是高危的患者—发展为综合症的机会是 20%—同样适用于经历相同程序而进行卵子捐献的妇女,我们相信, 针对高危妇女,提供可以接受的费用的情况下尽量消除 OHSS;我们应该努力研究并精密推算GnRH抑制剂和激动剂、IVM的实现程序。 然而目前尚缺乏大数据的前瞻性对照研究来证实方案的有效性,在现有方案的基础上尽可能做到完全避免OHSS 。
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心3525人已读 - 精选 AMH简介
抗苗勒氏管激素( anti-Müllerian hormone,AMH),又称苗勒管抑制物质,是属于转化生子超家族成员之一。两性性腺细胞均可分泌 AMH,但分泌期的量均不同。在雄性由睾丸未成熟的支持细胞分泌,具有使雄性胚胎苗勒氏管退化的作用;在雌性,其主要由窦前卵泡和小窦卵泡的颗粒细胞分泌,与卵巢功能密切相关,并调控卵泡生长和发育。抗苗勒氏管激素( AMH) 的生理作用1.抑制苗勒氏管的发育 在人类,性分化一般是从妊娠7w 开始,AM对两性胚胎期的苗勒氏管都有作用:在男性,当雄激素刺激午非氏管发育时,AMH则刺激成纤维细胞增生,促使苗勒氏管退化,而午非氏管分化为附睾管、输精管、精囊、射精管。在女性,由于缺乏雄激素和 AMH,使午非氏管退化而苗勒氏管发育为子宫、输卵管和阴道上段。2.调节性腺及生殖细胞的发育 AMH对两性性腺的发育起抑制作用:AMH在男性性分化中主要是使苗勒氏管退化, 并通过阻断睾丸Leydig 细胞的分化减少类固醇激素酶,作用于睾丸的发育并影响其功能; 出生后涉及性腺发育,生殖细胞的调控和诱导睾丸下降方面也起了一定的作用,AMH 对早期精子的形成和成熟亦有调节作用。在女性,AMH由出生后生长卵泡的卵巢颗粒细胞分泌,其抑制卵巢颗粒细胞上黄体生成激素受体及黄体酮的生物合成,调节卵子的发生及细胞的减数分裂,抑制颗粒细胞增殖和卵泡成熟,对成熟卵泡的选择有重要作用,在人类卵巢组织研究中,其在始基卵泡上无表达,在74%的初级卵泡的颗粒细胞上弱表达,在次级卵泡、窦前卵泡和 4mm的小窦卵泡中强表达,而在较大的窦卵泡( 4~8mm)中,AMH 的表达逐渐消失,在>8mm的卵泡中几乎无表达,在闭锁卵泡中亦无表达。人的小窦卵泡( 3~8 mm) 液中的AMH是排卵前卵泡的3 倍,卵巢有很高的芳香化酶的活性作用,能使睾酮转化为雄激素,而AMH能抑制颗粒细胞中 P450芳香化酶的合成,从而阻碍了雄激素向雌激素的转化,AMH并能使LH受体数量减少,抑制孕激素的产生。3.AMH其它作用 AMH有抑制某些肿瘤细胞生长和分化等的功能, 还具有抑制肺表面物质的积聚, 抑制胎儿肺成熟的作用。AMH在辅助生殖技术中的应用1. AMH 与卵巢储备功能 卵巢储备是指卵巢皮质区卵泡生长、发育,形成可受精卵母细胞的能力,表现为卵巢中存在的卵泡数量及其内卵子的质量,卵巢产生的卵母细胞数量和质量下降所致的生育力下降称为卵巢储备功能降低。在体外受精-胚胎移植过程中,评估卵巢储备功能,预测卵巢对促排药物的反应性是至关重要的前提,也是目前生殖医学面临的难题之一。 在超排卵过程中, 卵巢的反应性存在明显的个体差异,外源性促性腺激素刺激下可使不同患者卵泡发育的数量, 质量各不相同,卵巢的反应性主要由卵母细胞的数量和质量即卵巢储备功能决定。AMH 是由卵巢颗粒细胞分泌的活性因子,从始基卵泡池募集的卵泡在被选择成为优势卵泡前一直有 AMH 表达,其在初级卵泡的颗粒细胞上弱表达,在窦前卵泡和小窦卵泡的颗粒细胞中高表达, 而在始基卵泡 闭锁卵泡及卵泡膜细胞中则无表达。具有正常排卵功能的女性随着年龄增加,月经第3天血清 AMH 水平的改变要早于其他已知激素标志物,如抑制素 B和 FSH,提示血清 AMH 水平能更好地反映卵巢窦卵泡的数量,更准确地为月经正常但生育力下降的女性进行卵巢储备功能诊断。2.辅助生殖结局预测 随着辅助生殖技术的不断发展,IVF-ET成为治疗不孕症的重要手段,成功的IVF-ET临床妊娠是优质胚胎,正常的子宫内膜容受性和良好的内分泌水平共同作用的结果。近年来在女性生殖领域中,AMH受到了相当的重视,AMH与IVF治疗结局的关系有其特殊性,研究发现基础血清AMH水平是唯一能够预测IVF妊娠的因素。3.AMH和男性生殖精子发生是一个高度有序的细胞发育和分化过程,精子发生为激素依赖性过程,激素主要通过下丘脑一垂体一性腺轴调控精子发生,即下丘脑分泌的促性腺激素释放激素( GnRH)垂体分泌的卵泡刺激素( FSH)黄体生成素( LH)和睾丸间质细胞分泌的睾酮( T) 是精子发生的调节激素,但FSH和T等并不能直接作用于生精细胞,而是与睾丸支持细胞上的相应受体结合,产生效应因子,通过旁分泌作用营养生精细胞和调节生精过程。成年男性睾丸支持细胞产生AMH,精浆中存在AMH由于睾丸组织存在血睾屏障,大分子的AMH 不易溢出进入血循环,因而精浆AMH水平远高于血清水平,有学者研究发现精液正常者精浆AMH水平显著高于精液异常者,精浆AMH水平与精子密度、活动率等呈正相关。
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心2.9万人已读 - 医学科普 试管婴儿科普
我看过的,关于试管婴儿最好的科普,推荐给大家!https://mp.weixin.qq.com/s/gVgAB3qrTGUVeibv-jA5qQ
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心23人已读 - 原创 不孕不育就诊流程
 栾素娴 副主任医师 潍坊市人民医院 生殖医学中心42人已观看
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心42人已观看 - 医学科普 子宫输卵管造影小卡片
Hi,大家好,今天给大家介绍的是子宫输卵管造影子宫输卵管造影(hysterosalpingography)简称HSG,是一种常见的妇科检查方法,用于检查女性生殖系统是否正常,特别是不孕不育的患者。子宫输卵管造影通过注入一种特殊的造影剂来成像,能够清晰地显示子宫和输卵管的情况。首先在检查前,医生会先询问病史和体检,子宫输卵管造影需要在卵泡期进行,要求本次月经干净后不同房,一般月经规律的可以干净后3-7天,如果月经频发或者稀发,需要提前预约医生进行咨询;体格检查以确定是否有可能存在妇科疾病或生殖系统问题,如果有必要,还可能需要进行一些血液和阴道分泌物的检查。子宫输卵管造影的过程比较简单,通常在医院或妇产科专业的诊所进行。患者需要躺在检查床上,随后医生会严格消毒外阴以及阴道,暴露宫颈,宫颈插入一根专用的“子宫输卵管通水管”,通过导管注入造影剂,比较常见的造影剂是碘水或者碘油,然后进行X光拍片或其他成像检查。整个过程短暂,通常只需要几分钟。碘水造影:该检查使用的造影剂是碘水,是一种无色透明的水溶液,具有良好的碘化作用,可用于显示子宫和输卵管的情况。它的优点是造影效果好,代谢快,过敏反应较少;碘油造影:为生物不相容性较大的碘油,由于其体积大而黏稠,相对于碘水的注射会稍感不适和疼痛。碘油的密度比较高,图像显影比较清晰,但是层次感较差。子宫输卵管造影的最大优点是能够清晰地显示子宫和输卵管的情况,能够直观地了解子宫和输卵管是否通畅,有没有异常状况或阻塞。对于不孕不育的患者,这项检查能够提供重要的生育信息。此外,子宫输卵管造影过程中使用的造影剂通常是安全的,极少会引起过敏反应。当然,子宫输卵管造影也有一些缺点和注意事项。首先,这项检查并不能直接检查卵巢和卵子的情况,也不能准确检测是否存在某些生殖系统疾患者有其他可能存在的妇科问题,还需要进行其他检查。另外,部分患者可能会感觉到一些不适或疼痛,但这种感觉通常是短暂的,一般不需要特别的治疗。总之,子宫输卵管造影是一种重要的妇科检查方法,能够直观地了解子宫和输卵管的情况,对于不孕不育的患者更是提供了重要的生育信息。
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心42人已读 - 视频 人工授精小卡片
什么是人工授精?人工授精是一种辅助生殖技术,是通过医疗手段将男性的精子处理后直接用人工的方法放入女性的阴道、宫颈、或者宫腔内,从而达到受孕的目的。通常情况下,人工授精被视为一种比较简单的治疗不育症的方法。人工授精分为阴道内人工授精、宫颈内人工授精、宫腔内人工授精,我们一般是进行宫腔内人工授精;人工授精根据精液来源不同,还可以分为夫精人工授精和供精人工授精。人工授精的流程?在进行人工授精前,男性和女性必须接受一些身体检查,排除妊娠的禁忌症,从而尽量达到身体的最佳状态。在生殖医学专家的指导下,女性需要监测排卵,卵泡成熟以后,需要注射排卵针,在排卵前后24小时内男性提供精液样本,胚胎学家会将精液进行医学处理,生殖医学专家会通过医疗仪器将精液注入到女性的体内,以便在体内更容易达到女性生殖系统,从而达到受孕的目的。在人工授精之前,女性如果月经规律可以自然周期监测卵泡;如果月经不规律,可以采用医学促排卵的办法,让卵泡生长,然后卵泡成熟以后,可以注射排卵针,以激活排卵过程,从而增加成功受孕的机会。人工授精的成功率是多少?人工授精的成功率通常取决于许多因素,如年龄、生殖健康状况和生育计划。在最佳条件下,人工授精的成功率可以达到10%至20%左右。然而,在某些情况下,如果患者单纯性功能障碍,可能怀孕率会升高,当然,如果双方还存在一些不明原因的不孕因素,则人工授精的成功率可能会更低,或者医生可能会建议使用其他辅助生殖技术。人工授精有哪些风险和并发症?大多数情况下,人工授精是安全有效的。然而,就像其他医疗过程一样,人工授精也会有一些风险和并发症。常见的风险包括宫外孕、感染、多胎妊娠等。但是,如果按照建议方式进行人工授精,尽可能遵守医生的建议,可以最大限度地降低这些风险。结语:人工授精是一种常见的辅助生殖技术,是一种治疗男性和女性不育症的有效方法,它可以帮助许多人实现梦想成为父母。然而,人工授精并不是所有情况都适用。如果你存在不孕的情况,或者正在考虑进行人工授精,最好与生殖医学专家进行咨询,以便了解自己的治疗选项和选择最适合自己需求的辅助生殖技术。
 栾素娴 副主任医师 潍坊市人民医院 生殖医学中心暂无购买
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心暂无购买 - 遗传病 进行性肌营养不良
近期有肌营养不良的病人咨询试管婴儿,特意整理一下,分享给大家。进行性肌营养不良(Progressivemusculardystrophy)是一组以骨骼肌进行性无力萎缩为主要临床表现的异质性基因缺陷性疾病。可伴有中枢神经系统、心脏、骨骼、呼吸及胃肠道受累。不同类型起病时间、进展速度、受累范围、严重程度差异很大。遗传方式分为X连锁隐性遗传、常染色体显性遗传、常染色体隐性遗传等。以DMD为例:Duchenne/Becker型肌营养不良遗传方式为X连锁隐性遗传,发病率在各个国家、地区和人种间无明显差异,每3600~6000出生男婴中有1例发病。我国的发病率约为1/3853,估算全国患者约70000人。X连锁隐性遗传,男性患儿发病,患儿母亲为隐形携带者,她生育子女中,女孩表型正常,一半是携带者,男孩一半患病,如果准备再次生育,建议选择三代试管,挑选健康囊胚移植。其它遗传模式相同道理,首先明确遗传基因以及遗传模式,其次建议三代试管。
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心70人已读 - 患者故事 ivf助孕故事(一)
2019年9月8日,娜娜走进了我的诊室,询问病史的时候,她有点腼腆,不知道从何处开始讲起,于是,我慢慢的引导着,听她一一道来:1988年4月娜娜出生在日照一个普通的工人家庭,从小就体弱多病,营养不良,4岁时因为感冒住院,查体时发现室间隔缺损,因为当时太小了,一直没有手术,7岁父母带着她到北京做了室间隔修补术。之后娜娜的身体慢慢好了起来,个头在同龄孩子中也算比较高的,14岁初三的时候因为急性腹痛在当地医院就诊,因急腹症行剖腹探查术,术中发现“卵巢良性畸胎瘤扭转坏死、急性化脓性阑尾炎”行阑尾切除术+左侧卵巢切除术。术后尽管只有一个卵巢,但娜娜恢复挺快,平时月经也比较规律,日子顺风顺水,娜娜大学毕业,做了一名人民教师,日益繁重的工作,让刚刚二十几岁的她鬓角出现了几许白发....2017年娜娜结婚,她的爱人也是一名教育工作者,两人琴瑟和谐,生活美满,唯一的缺憾就是没有宝宝,娜娜又想起以前做过的手术,难道真是手术引起的不孕吗?于是小两口从此开始了艰难的求子之路,2019年9月娜娜在当地医院做了子宫输卵管造影:子宫形态正常,右侧输卵管伞端粘连并积水、不通表现,左侧输卵管梗阻;面对这样的结果,娜娜哭了,难道这一生真的没有宝宝了吗?带着这样的问题,娜娜夫妇从日照来到潍坊。根据情况,我当时给娜娜做了卵巢储备功能的评估,基础内分泌:FSH8.78IU/L,LH4.44IU/L,E276.4pmol/L。AMH:1.04ng/ml。B超:右侧卵巢AFC3个。男方精液大致正常。建议行ivf助孕。 2019年11月第1次取卵,采用拮抗剂方案,获卵6枚,2PN2枚,多PN4枚,未移植,冻存1枚胚胎。分析这个周期的情况,娜娜出现了异常受精,正常卵子在受精的时候要出现皮质反应,也就是说卵子的透明带只能让第1个精子穿过,防止第2个第3个精子穿过,而由于卵巢储备功能减退,卵子的皮质反应减退,导致出现多精受精的情况,建议再次取卵改行二代试管,即采用卵泡浆内单精子注射技术;于是2020年5月于我中心行第2周期取卵,本周期采用长方案,获卵1枚,卵子畸形。又一次的打击,娜娜几乎绝望了,难道真的命中注定没有孩子吗?娜娜的老公是个非常豁达的小伙子,多次表示,人生不是有孩子才完美,趁着年轻是应该努力尝试;于是,在经过一系列的调理之后,2020年8月娜娜第3次取卵,此时她的卵巢储备功能已经很差,AMH0.44ng/ml,功夫不负有心人,这一次采用微刺激方案,一共取到了6枚卵,采用卵泡浆内单精子注射技术,受精5枚,形成2枚可移植胚胎,冻存。 至此,娜娜总共积攒了3枚D3天的胚胎,根据她的年龄和胚胎分级,我们建议她可以考虑移植,但是,在试管婴儿术前检查时发现娜娜的血压偏高;经过高血压科门诊以及心内科门诊医生各种详细的检查,确认是原发性高血压,2级,中危,建议系统治疗,控制好血压以后移植,于是,娜娜开始限盐、控制体重,锻炼身体,经过几个月的观察,血压仍然偏高,之后开始口服拉贝洛尔,取卵后半年,娜娜终于开始准备移植了。 2021年全国的疫情形势很紧张,各地纷纷对外来人员采取核酸检测、隔离管控等措施,娜娜所在的地区出现阳性的患者,很长一段时间都不能出门;在这种焦虑、封闭的环境中,娜娜又出现了新的状况;在一次腹痛后,娜娜在当地医院行妇科B超,发现右侧输卵管积水增大,同时可能有化脓的可能,于是再次和我联系,考虑到输卵管积水可能在胚胎移植后反流进入子宫,从而影响胚胎着床,建议娜娜手术结扎右侧输卵管,因为疫情的原因,娜娜夫妇俩选择到省城医院进行手术,谁料到,疫情不作美,在预约的时间里,本省的疫情再次加重,手术计划只能取消。 困于家中,日益的焦虑,娜娜的输卵管积水再次发作,2021年12月因为不明原因的发热于当地市级医院就诊,检查过程中:发现子宫肌瘤,双侧输卵管积液可能;排除各种原因,考虑盆腔感染引起,于是在当地医院抗感染治疗;治疗10余天,效果不明显,娜娜再次返回我们医院,这次在妇科病房住了7天,经过药敏试验,采用哌拉西林他唑巴坦结合中药治疗后好转出院。 回到家中,娜娜谨遵医嘱,坚持运动锻炼,娜娜的老公更是变着法的给她加强营养。2022年4月疫情缓解的时候,夫妇俩个重新返院,准备手术治疗;经过详细的评估,同时请妇科医生会诊,决定行腹腔镜下右侧输卵管结扎+左侧输卵管切除+盆腔粘连松解+宫腔镜检查+诊断性刮宫术,手术非常顺利,娜娜又开始了新的期待。 术后一月,娜娜经过门诊复查,正式进入冻胚移植的程序;首先是子宫内膜准备,内膜厚度形态都符合移植要求,于是,2022-06-25,这个改变命运的日子,冻胚移植了,好事多磨,历尽千帆,终于修得正果,2022-07-09,移植后第14天,HCG结果471.7miu/ml,彼时,我看见这个坚强勇敢的姑娘眼里泛着泪花.... 十个月的长征啊,仅仅开始了第一步,接下来的每一天都是考验。移植后28天于我院行彩超提示宫内早孕。之后每两周复诊1次,每次复诊主要是产科B超检查,一次次看着屏幕上那个小小的生命,感受他一天天的长大,娜娜的心激动极了! 因为得来不易,娜娜严格遵守医生的嘱咐,定期产检,胎儿NT、无创DNAPLUS、胎儿系统超声、心脏超声.....娜娜一步一步,过关斩将,胎儿关关告捷,但是因为之前的高血压,娜娜的身体频繁报警,先是孕期血糖筛查结果异常、之后是孕期蛋白尿、反复的子宫收缩,娜娜总共在产科住院4次,孕期用的药更是从来没有停过,从开始人工周期的雌孕激素药物、到降压药物、改善微循环的药物、抗凝的药物、防止宫缩的药物、促进胎肺成熟的药物、加强营养的药物..... 终于,34岁的娜娜迎来了她人生中最最难忘的日子,2023-02-22,因“1.妊娠期糖尿病;2.慢性高血压并发子痫前期;3.妊娠合并子宫肌瘤;4.妊娠合并高脂血症;5.37周妊娠;6.脐带绕颈;7.左侧附件切除术后;8.右侧输卵管结扎术后;9.室间隔缺损修补术后;10.阑尾切除术后;11.IVF-ET术后"于2023-02-22在腰硬联合麻醉下行子宫下段剖宫产术,术中以LOA位剖一男婴,评10分,外观发育正常,手术顺利,母子平安! 看着娜娜发来的宝宝的照片,我的眼泪慢慢落下,人生诸多不易,只有经历才知道。随笔写下这段文字,一是感谢我的病人,你们的持之以恒才是我坚持的动力,感谢信任,感谢相遇。二是送给娜娜和她老公,人生的路很长,永远记住这一段你们相互扶持相互勉励的日子,且行且珍惜,祝愿将来的日子更美好。
栾素娴 副主任医师 潍坊市人民医院 生殖医学中心暂无购买





